Translational Diabetes
Wir untersuchen, wie äussere Einflüsse und Umweltfaktoren – wie etwa eine fettreiche Ernährung oder Luftverschmutzung – das Immunsystem im Darm beeinflussen und dadurch unsere Gesundheit, insbesondere den Stoffwechsel (z.B. Körpergewicht und Diabetesrisiko), verändern können.
AG Cavelti-Weder / Translational Diabetes
Das Exposom beschreibt die Gesamtheit aller Umweltfaktoren, denen ein Mensch im Laufe seines Lebens ausgesetzt ist. Dazu zählen exogene Einflüsse wie die Nahrung, die wir zu uns nehmen, oder Luftschadstoffe, die wir einatmen, aber auch endogene Faktoren wie das Mikrobiom im Darm. Diese Umweltfaktoren wirken im Zusammenspiel mit der genetischen Prädisposition und beeinflussen massgeblich unsere Gesundheit.
In unserer Arbeitsgruppe untersuchen wir ausgewählte Komponenten des Exposoms und deren Einfluss auf das intestinale Immunsystem. Besonders interessiert uns, wie Ernährung, Schadstoffpartikel, Weichmacher oder Infektionserreger über das Immunsystem im Darm Entzündungsprozesse auslösen können und so zur Entstehung weit verbreiteter Stoffwechselerkrankungen wie Übergewicht und Diabetes beitragen.
Mit Hilfe von in vivo Mausmodellen und translationaler Studien am Menschen analysieren wir die Veränderungen des angeborenen und adaptiven Immunsystems im Darm im Zusammenhang mit Übergewicht und Diabetes. Darüber hinaus sind wir an den zugrunde liegenden Mechanismen dieser Krankheitsprozesse interessiert und ob die damit verbundenen immunologischen Veränderungen im Darm durch Gewichtsreduktion reversibel sind.
Diese Erkenntnisse liefern neue Einblicke in die Immunfunktionen des Darms und bilden die Grundlage für gezielte Interventionen gegen umweltbedingte Stoffwechselerkrankungen.
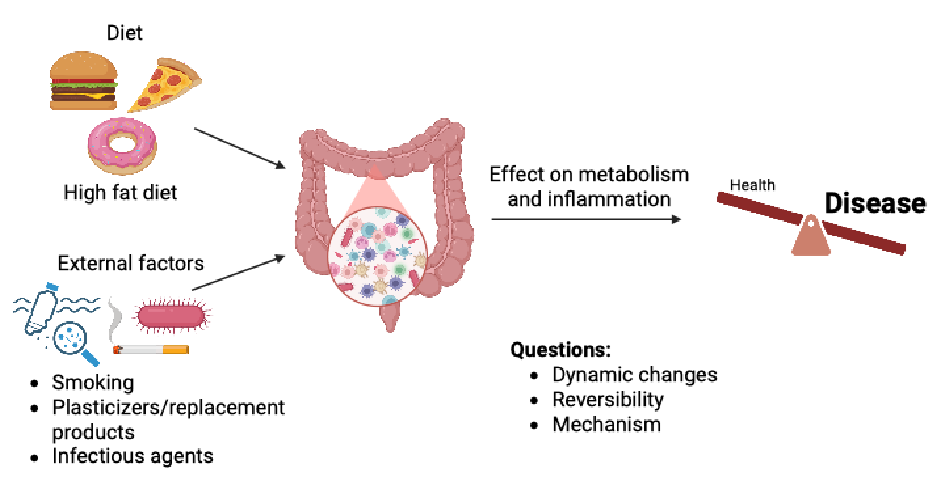
Forschungsthemen
Grundlagenforschung I: Rolle der Ernährung in der Darm(patho)physiologie und metabolische Folgen
Stoffwechselerkrankungen wie Adipositas und Diabetes werden zunehmend als komplexe Erkrankungen anerkannt, die durch genetische, ernährungsbedingte und umweltbedingte Faktoren ausgelöst werden. Dabei spielt die Ernährung eine entscheidende Rolle bei der Modulation der Schleimhautimmunität mit Auswirkungen auf die Glukosehomöostase und die Stoffwechselgesundheit. Wir haben gezeigt, dass eine fettreiche Ernährung zu einer Zunahme entzündlicher Makrophagenpopulationen im Darm von Mäusen führt [1]. Wir haben diese Ergebnisse auf den Menschen übertragen und bestätigt, dass Adipositas und eine ungesunde Lebensweise die Immunzellpopulationen im menschlichen Darm verändern [2]. Die spezifische Depletion von Makrophagen im Dickdarm von Mäusen, die mit einer fettreichen Ernährung gefüttert wurden, führte zu einer verbesserten Glukosetoleranz, was einen kausalen Zusammenhang zwischen Makrophagen im Dickdarm und der Glukosehomöostase bestätigt [1]. Eine langfristige umfassende Analyse der Darmimmunität bei Adipositas, ihrer potenziellen Reversibilität und der mechanistischen Zusammenhänge ist jedoch noch wenig verstanden.
Wir wollen verstehen, wie eine fettreiche Ernährung die Immunzellpopulationen im Darm beeinflusst und wie diese Veränderungen zu Stoffwechselstörungen beitragen. Das ultimative Ziel ist es, mechanistische Erkenntnisse in neue therapeutische Strategien zur Verbesserung der Stoffwechselgesundheit und zur Prävention von Diabetes zu übertragen.
Spezifische Projekte:
- Dynamische Veränderungen der Darmimmunzellen bei Adipositas im Zeitverlauf
- Auswirkungen von Nahrungsfetten auf die Glukosehomöostase und Immunzellen
- Auswirkungen von Gewichtsverlust auf Immunzellpopulationen
- Mechanismus der durch fettreiche Ernährung induzierten Interferonreaktion
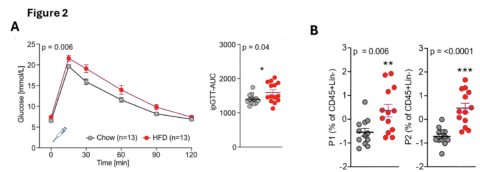
Abbildung 2: Glukoseintoleranz und entzündliche Makrophagen bei Mäusen, die eine fettreiche Ernährung im Vergleich zu einer Standardernährung erhielten. (A) Glukosetoleranztest von Mäusen nach einer Woche fettreicher Ernährung (rot) im Vergleich zu Mäusen mit Standardernährung (grau). (B) Z-Score der Häufigkeit proinflammatorischer Makrophagenpopulationen P1 und P2, normalisiert auf CD45+-Zellen.
Grundlagenforschung II: Rolle von Umweltfaktoren in der Darm(patho)physiologie und metabolische Folgen
Neben den allgemein bekannten Risikofaktoren für Diabetes wie Ernährung, Lebensstil und Genetik sind mehrere Umweltfaktoren bekannt, die das Diabetesrisiko erhöhen. So wurden beispielsweise Luftverschmutzung und Rauchen sowohl in epidemiologischen Studien [3-6] als auch in Studien an Nagetieren [7, 8] als Risikofaktoren für Diabetes identifiziert. Traditionell wurden die Lungen als das primär von diesen Schadstoffen betroffene Organ angesehen. Die Rolle des Magen-Darm-Trakts wurde jedoch weitgehend übersehen, obwohl es Hinweise darauf gibt, dass diese Partikel über die mukoziliäre Clearance aus der Lunge und durch direkte Aufnahme über kontaminierte Lebensmittel in den Darm gelangen. Um die nachgelagerten metabolischen Folgen der Exposition von Lunge und Darm gegenüber Luftverschmutzung zu bestimmen, setzten wir Mäuse Luftverschmutzungspartikel direkt in der Lunge (intratracheale Instillation) oder im Darm (Sondernahrung) aus. Wir fanden heraus, dass die orale, aber nicht die intratracheale Exposition gegenüber Luftverschmutzungspartikel ein entzündliches Milieu im Darm mit anschließender Betazelldysfunktion induzierte [9]. Mechanistisch führte die orale Exposition gegenüber Luftverschmutzungspartikel zu einer Verringerung der entzündungshemmenden/residenten Makrophagen und zu einer Interferon- und Entzündungssignatur in den Makrophagen des Dickdarms [10]. Die Depletion von Makrophagen, NLRP3 oder IL-1β schützte Mäuse vor luftverschmutzungsinduzierter Glukoseintoleranz, was ihre Beteiligung an der Pathogenese der Erkrankung belegt [10].
Mehrere Umweltfaktoren wurden mit einem erhöhten Diabetesrisiko in Verbindung gebracht. Unser Ziel ist es, zu untersuchen, ob die beteiligten Mechanismen denen von Luftverschmutzungspartikel ähneln, nämlich durch die Induktion eines entzündlichen Milieus im Darm.
Spezifische Projekte:
- Orale Exposition gegenüber Zigarettenrauchpartikeln und metabolische Dysregulation
- Die Rolle von Weichmachern und Ersatzprodukten bei Stoffwechselerkrankungen
- Der Darmprotozo Trichomonas musculus und die Glukosehomöostase
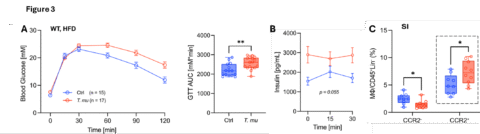
Die T. mu-Kolonisierung bei Wildtyp-Mäusen, die mit einer fettreichen Ernährung gefüttert wurden, führt zu einer gestörten Blutzuckerkontrolle, erhöhter Insulinsekretion und Darmentzündungen. (A) Intraperitonealer Glukosetoleranztest (ipGTT), Fläche unter der Kurve (AUC) von mit T. mu-Kolobisierung (rot) und nicht kolonisierten (blau) Mäusen. (B) Zirkulierendes Insulin, gemessen während der ersten 30 Minuten des ipGTT. (C) Entzündliche CCR2+-Makrophagen im distalen Dünndarmgewebe.
Translationale Studien auf der Grundlage von Grundlagenforschung
Unser übergeordnetes Ziel ist es, eine Brücke zwischen präklinischer Forschung und translationalen Anwendungen zu schlagen, indem wir Ergebnisse in Studien am Menschen validieren. Ein Beispiel für diesen Ansatz ist unsere Arbeit zur mukosalen Immunität bei Mäusen mit fettreicher Ernährung [1], die wir erfolgreich auf den Menschen mit Adipositas übertragen konnten [2]. Wir haben außerdem zwei Mausmodelle für Gewichtsreduktionsoperationen etabliert und nachgewiesen, dass ein langer biliopankreatischer Arm metabolisch einem kurzen Arm überlegen ist [11, 12]. Um diese Erkenntnisse in einen klinischen Kontext zu übertragen, untersuchen wir die metabolischen und immunologischen Auswirkungen eines kurzen gegenüber einem langen biliopankreatischen Schenkel bei menschlichen Patienten, die sich einer bariatrischen Operation unterziehen. Darüber hinaus verwenden wir RNA-Sequenzierungsdaten aus peripheren mononukleären Blutzellen von Patienten nach einer Gewichtsreduktionsoperation, um frühe Biomarker für eine Verbesserung des Stoffwechsels zu identifizieren. Parallel dazu analysieren wir einen bestehenden Datensatz zum Darmmikrobiom, um die translationale Relevanz unserer präklinischen Erkenntnisse zur Rolle von Trichomonas-Spezies im Glukosestoffwechsel zu bewerten.
Damit wollen wir die Reversibilität von Veränderungen der Immunzellen nach einer Gewichtsreduktionsoperation und den Zusammenhang zwischen Trichomonas-Arten und dem Diabetesrisiko beim Menschen verstehen.
Spezifische Projekte:
- Auswirkungen einer Gewichtsreduktionsoperation auf Darmimmunzellen (SLIM-Studie)
- Auswirkungen einer Gewichtsreduktionsoperation auf das Bluttranskriptom
- Trichomonas und Glukosehomöostase beim Menschen
Klinische Studien
Als leitende Ärztin der Klinik für Endokrinologie und klinische Ernärhung am Universitätsspital Zürich leite ich mehrere Studien mit Schwerpunkt auf der stationären und ambulanten Diabetesversorgung. Die Forschungsfragen, mit denen wir uns befassen, leiten sich direkt aus klinischen Herausforderungen und ungedecktem Bedarf ab und zielen darauf ab, das Patientenmanagement zu verbessern, therapeutische Strategien zu optimieren und innovative Technologien in die Diabetesversorgung zu integrieren. Ein wichtiger Bestandteil dieser Bemühungen ist das nationale Diabetesregister SwissDiab, an dem ich als Vorstandsmitglied aktiv mitwirke. Dieses Register ist eine wertvolle Quelle für Längsschnittdaten von ambulant behandelten Diabetespatienten.
Konkrete Projekte
- SwissDiab-Register: Patientenergebnisse
- Von Patienten berichtete Ergebnisse wie Lebensqualität im Zusammenhang mit Diabeteskomplikationen,
- Die Anwendung von Finerenon bei Typ-2-Diabetes,
- Off-Label-Anwendung von GLP-1-Rezeptoragonisten bei Typ-1-Diabetes,
- Wirkung von GLP-1-Rezeptoragonisten bei metabolisch bedingter steatotischer Lebererkrankung (MASLD).
- Kontinuierliche Glukosemonitoring-Daten für die erweiterte glykämische Bewertung
- C-Peptid/Glukose-Verhältnis zur Früherkennung von Diabetes bei Mukoviszidose
- Personalisierte Insulindosierung durch maschinelles Lernen
- Octopatch: Ein bukkales Pflaster zur Verabreichung von Peptidwirkstoffen
Kooperationen
- M. Rothenbühler, A. Lizoain (DCB Bern)
- D. Klein Cerrejon und Dr. N. Paunovic (ETH/ OBaris)
- M. Brändle, HOCH
- A. Odermatt (Universität Basel)
- P. Vonaesch (Universität Lausanne)
- S. Erttmann (Universität Kiel)
- N. Perakakis (TU Dresden)
- R. Peterli und Dr. R. Schneiter (Viszerale Chirurgie, Universität Basel)
- M. Scharl und Prof. L. Biedermann (Gastroenterologie, USZ);
- N. Bukolich (ETH ZH)
- P. Schär (Universität Basel)
- J. Roux (Universität Basel)
- K.-H. Herzig (Universität Oulu)
- M.-R. Jarvelin (Kings College London)
- A. Blakemore (Brunel University)
- M. Krauthammer (Universität Zürich/ USZ)
Finanzierung
- SCAHT-Forschungsprogramm 2025–2028, Co-PI
- Internationale Graduiertenkolleg (IRTG) zwischen der Technischen Universität Dresden, der Universität Zürich und der ETH Zürich
- Innovationspool USZ
- SNSF, Projektförderung (320030_219851)
- SNSF, Projektzuschuss (32003B_204937), Co-PI
- Vontobel-Stiftung



